ترکیبات آلی فلزی به ترکیبات شیمیایی میگویند که حداقل شامل یک پیوند بین عنصری فلزی و اتم کربن متعلق به یک مولکول آلی باشد. حتی عناصری فلزی همچون سیلیکون (سیلیسیم)، قلع و بور میتوانند ترکیبات آلی فلزی ایجاد کنند که در صنعت، استفادههای بسیاری از آنها میشود. کاتالیز واکنشهایی که مولکول هدف در آنها شامل پلیمر یا مواد دارویی باشند به کمک ترکیبات آلی فلزی امکانپذیر است که در نهایت، موجب افزایش سرعت واکنش میشوند.
به طور کلی، پیوند بین اتم فلزی و کربن متعلق به مولکول آلی، از نوع پیوند کووالانسی است. زمانیکه فلزاتی همچون سدیم و لیتیوم با الکترونگاتیوی کم، ترکیبات آلی فلزی را ایجاد کنند، خاصیتی کربانیونی توسط اتم کربن متصل به فلز مرکزی دیده میشود.
شیمی ترکیبات آلی فلزی
شیمی آلی فلزی به مطالعه ترکیباتی اختصاص دارد که شامل واکنش در پیوندهای کربن-فلز هستند. این نوع از پیوند کربن-فلز ممکن است موقتی باشد اما اگر در طول یک واکنش یا در یک ترکیب مورد نظر، چنین پیوندی داشته باشیم، واکنش ما مرتبط با شیمی ترکیبات آلی فلزی خواهد بود. فارغ از اهمیت وجود پیوند کربن-فلز، پیوند بین فلزات و سایر عناصر معمول در شیمی آلی نیز با شیمی ترکیبات آلی فلزی پیوند خورده است. از جمله چنین پیوندهایی میتوان به موارد زیر اشاره کرد:
پیوند نیتروژن-فلز
پیوند اکسیژن-فلز
پیوند هالوژن-فلز
پیوند هیدروژن-فلز
همانطور که میدانید، فلزات، بخش اعظمی از جدول تناوبی را شکل میدهند و شامل فلزات قلیایی (گروه اول)، فلزات قلیایی خاکی (گروه دوم)، فلزات واسطه (گروه ۳-۱۲)، فلزات گروه اصلی (گروههای ۱۳-۱۵) و همچنین، لانتانیدها و اکتینیدها هستند. در این مطلب، بیشتر بر روی رفتار فلزات واسطه تمرکز میکنیم چراکه در حقیقت، این فلزات، شرایط الکترونگاتیو و غیرالکترونگاتیو سایر عناصر را پوشش میدهند.
اهمیت مطالعه ترکیبات آلی فلزی
مطالعه ترکیبات آلی فلزی از آن جهت اهمیت دارد که این ترکیبات در سنتز، بسیار انعطافپذیر هستند. در حقیقت، واکنشها و تغییراتی که با ترکیبات آلی فلزی انجام میگیرند را نمیتوان با سایر ترکیبات آلی انجام داد. به طور مثال، تصویر زیر را در نظر بگیرید. تشکیل پیوند بین حلقه فنیل در شیمی آلی غیرقابل تصور است اما اگر با شیمی ترکیبات آلی فلزی آشنا باشیم، این واکنش، بسیار ساده انجام میگیرد.
ترکیبات آلی فلزی
برومو بنزن، الکتروفیلی مستعد به نظر میآید و اگر با هیدروکربنها آشنا باشید، فنیل برونیک اسید را نوکلئوفیلی مستعد در نظر میگیرید. کاتالیزور پالادیم سبب وقوع چنین واکنشی میشود. به بیان سادهتر، این ترکیبات آلی فلزی هستند که گستره واکنشهای شیمیایی را برای یک شیمیدان، وسعت میبخشند. لازم به ذکر است که شیمی آلی فلزی مملو از کشفیات متعدد است که مطالعه آنرا برای تمامی اشخاص، شگفتانگیر میکند.
سنتز ترکیبات آلی فلزی
در ادامه این مطلب، روشهای مختلف تهیه ترکیبات آلی فلزی را بررسی میکنیم.
فلزات و هالیدهای آلی
واکنش یک فلز با یک هالید آلی، روش مناسبی برای سنتز ترکیبات آلی فلزی به شمار میآید که در این نوع از واکنشها، فلز به طور معمول، لیتیم، منیزیم و روی است. اترها، به طور ویژه دیاتیل اتر و تترا هیدروفوران، محیطی خنثی و قدری قطبی را فراهم میکنند که در این شرایط، ترکیبات آلی فلزی به صورت محلول وجود دارد. رطوبت، اکسیژن و دیاکسید کربن را باید از محیط واکنش حذف کرد چراکه با ترکیب مورد نظر وارد واکنش میشوند. برای اینکار از اتمسفری خنثی همچون نیتروژن یا هلیوم استفاده میشود. در زیر، به ترتیب واکنشهای سنتز متیل لیتیوم و اتیل منیزیم برمید را مشاهده میکنید.
.
CH3Br+2Li⟶(CH3CH2)2OCH3Li+LiBr
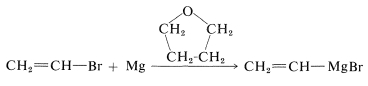
CH3CH2Br+Mg⟶(CH3CH2)2OCH3CH2MgBr
واکنشپذیری هالیدها از روند زیر پیروی میکند:
منیزیم و لیتیوم به خوبی با کلریدها، برمیدها و یدیدها واکنش میدهند اما روی، تنها با برمید و یدید وارد واکنش میشود. جیوه نیز تنها زمانی که به صورت آمالگام (ملغمه) با سدیم باشد، وارد واکنش میشود. سدیم و پتاسیم، به علت واکنشپذیری بالای آلکیل سدیم و آلکیل پتاسیم، مشکلاتی در سنتز ترکیبات آلی فلزی شامل اتر و هالیدهای آلی بوجود میآید.
هالیدهای آلکنیل، آلکینیل و آریل را همچون آلکیل هالیدها میتوان به ترکیبات شامل لیتیوم و منیزیم متناظر با خود تبدیل کرد. با این وجود، شرایط واکنش، از جمله نحوه انتخاب حلال، اهمیت بسیار زیادی دارد.
هالیدهای واکنشپذیر آلیلی و بنزنی، مشکلاتی را در سنتز ترکیبات آلی فلزی ایجاد میکنند. از جمله واکنشهای جانبی ناخواسته در تهیه این نوع از ترکیبات، واکنش جابجایی از نوع SN2است.
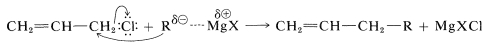
برای کاهش این اثر، از مقدار اضافه منیزیم و رقیقسازی محلول هالیدهای آلیلی استفاده میشود. در آمادهسازی ترکیبهای آلکیل سدیم نیز با چنین مشکلی مواجه هستیم. هالید آغازگر RXبا RNA
جفت میشود یا اینکه به یک آلکن تبدیل خواهد شد. چنین واکنشهایی سبب تولید رادیکالهای آزاد میشوند.
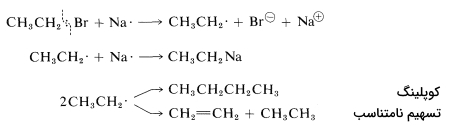
در غیاب سدیم فلزی، اتیل سدیم با اتیل برمید واکنش میدهد. دلیل این اتفاق این است که آنیون CH3CH2
، تمایل به از دست دادن الکترون دارد و همچون اتم سدیم فلزی، با دادن یک الکترون به CH3CH2BR
، یک رادیکال اتیل تولید میکند و خود نیز به رادیکال اتیل تبدیل میشود. رادیکالهای ایجاد شده در نهایت میتوانند در تولید بوتان، اتان و اتن نقش داشته باشند.
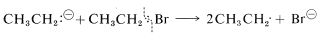
این که انتظار داشته باشیم با تغییر ساختار هالیدها و طبیعت فلز، سرعت واکنشهای SN2, E2
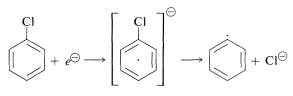
از سرعت واکنشهای رادیکالی بیشتر باشد، هنوز به درستی تعیین نشده است. با این وجود، مشخص شده است که واکنشهای جانشینی در آریل هالیدهای غیرفعال وجود دارند که بدون بازآرایی (نوآرایی) و به کمک واسطهای رادیکالی انجام میشوند.
مرحله اساسی در این نوع از واکنشها، دادن یک الکترون به یکی از اوربیتالهای پرنشده پای در حلقه و خروج یک یون هالید است.
سایر روش های تولید ترکیبات آلی فلزی
در ادامه، روشهایی برای سنتز ترکیبات آلی فلزی مطرح میشوند که معمول نیستند اما از جمله روشهای کاربردی به شمار میروند. در هر یک از این روشها، حلال باید نسبت به تمامی ترکیبات آلی فلزی شرکت کننده، خنثی باشد.
تبادل فلز و هالوژن
واکنش کلی در این روش، به صورت زیر است:
تعادل در این نوع از واکنشها به طرف تولید ترکیبات آلی فلزی است و اتم فلزی به گروه R با الکترونگاتیوی بیشتر متصل است. این روش به طور عمده در تهیه ترکیبات آلی فلزی مشتق شده از هالیدهای غیرواکنشپذیر همچون هالیدهای آریل، اتنیل یا اتینیل مورد استفاده قرار میگیرد.

جانشینی یک فلز با دیگری
در اینجا، تعادل به گونهای است که گروه R، به فلز با الکترونگاتیوی کمتر متصل میشود.
واکنش ترکیبات آلی فلزی با هالیدهای فلزی
در این واکنشها، فرآوردهای تولید میشود که در آن، گروه R به فلزی با الکترونگاتیوی بیشتر متصل باشد و بنابراین، در اثر واکنش، ترکیب آلی فلزی با واکنشپذیری پایین نسبت به ترکیب قبل خواهیم داشت.
تولید به کمک هیدروکربن های اسیدی
برخی از ترکیبات آلی فلزی را میتوان از طریق واکنش با یک باز قوی یا مشتق یک آلکیل فلزی، با هیدروکربنی اسیدی همچون یک آلکین تولید کرد.
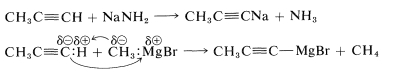
از جمله مثالهای این روش میتوان به ترکیب ۱و۳-سیکلوپنتادین اشاره کرد که به دلیل باز مزدوج خود (آنیون سیکلوپنتادین)، به خوبی از طریق پخش شدگی (غیرمتمرکز شدن) الکترون، به پایداری میرسد. آنیون به راحتی به کمک واکنش هیدروکربن و متیل لیتیوم تشکیل میشود.

سنتز ترکیبات آلی فلزی به کمک ترکیبات پلی هالوژن
اگر هالوژنها در دیهالیدها با سه پیوند کربن-کربن یا کمتر از یکدیگر جداشده باشند، نمیتوان «ترکیبات آلی فلزی دوتایی» (Diorganometallic Compounds) را نمیتوان به کمک دیهالیدها تهیه کرد چراکه به طور معمول، واکنش حاکم به صورت حذفی خواهد بود. با فلزات فعال و دیهالیدهایی که نام آنها به صورت ۱و۱-، ۱و۲- یا ۱و۳ باشند، واکنشهای زیر را خواهیم داشت:
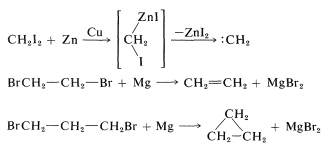
زمانیکه هالوژنها حداقل به میزان ۴ اتم کربن با یکدیگر فاصله داشته باشند، ترکیبات آلی فلزی دوتایی شکل میگیرند:
کربِنها (کاربن) با فرمولR2C
را به کمک واکنش حذفی آلفا و از طریق ترکیبات پلیهالوژن میتوان تولید کرد که در این واکنشها، از ریجنتهای آلیفلزی بهره میگیرند. در مرحله اول، تبادل هالوژن-فلز و در ادامه، حذف هالید فلزی را خواهیم داشت.

واکنشهای حذفی از این دست برای سنتز و تشکیل پیوندهای کربن-کربن مناسب هستند. به طور مثال، در حضور یک آلکن، دیبرمو کربِن تولید میشود که با شرکت در «واکنشهای حلقهافزایی» (Cycloaddition Reaction)، مشتقات سیکلوپروپان تولید میشود.

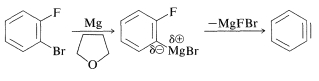
از نمونههای این سنتز میتوان به تولید «بنزین» (Benzyne) از ۱-برمو-۲-فلوئوروبنزن به کمک منیزیم در تتراهیدروفوران اشاره کرد. اگر دما در حدود صفر درجه سانتیگراد حفظ شود، ۲-فلوئوروفنیل منیزیم برمید تشکیل میشود. در دماهای بالاتر، هالید منیزیم حذف و بنزین به تولید میرسد.
خواص ترکیبات آلی فلزی
در ادامه به طور خلاصه به بررسی خواص ترکیبات آلی فلزی میپردازیم.
پیوند بین فلز و اتم کربن، به طور معمول، طبیعتی به شدت کووالانسی دارد.
بیشتر ترکیبات آلیفلزی، خاصه ترکیباتی که گروههای هیدروکربنی به صورت آروماتیک یا شامل ساختار حلقوی باشند، به حالت جامد وجود دارند.
ترکیباتی شامل اتمهایی با الکترونگاتیوی بسیار کم (همچون سدیم و لیتیوم)، به شدت فرار هستند و در واکنشهای سوختن خودبهخودی شرکت میکنند.
در بسیاری از موارد، ترکیبات آلی فلزی بویژه ترکیبات فرار، برای انسانها سمی هستند.
این نوع از ترکیبات، بویژه آنهایی که از طریق فلزاتی با الکترونگاتیوی کم تولید شدهاند، میتوانند نقش عامل کاهنده داشته باشند.
با توجه به مسائل مطرح شده در بالا میتوان دریافت که خواص ترکیبات آلی فلزی به خواص فلزات تشکیل دهنده آنها وابسته است.
کاربرد ترکیبات آلی فلزی
ترکیبات آلیفلزی، کاربردهای گستردهای در زمینه شیمی دارند که در ادامه به برخی از آنها اشاره شده است:
در برخی از واکنشهای تجاری شیمی، از ترکیبات آلی فلزی به عنوان کاتالیزورهای همگن استفاده میشود.
این نوع از ترکیبات به عنوان ریجنتهای استوکیومتری در واکنشهای شیمیایی صنعتی و تحقیقاتی به کار گرفته میشوند.
در تولید بعضی از نیمههادیها و «الایدیها» (LEDs) از این ترکیبات بهره میگیرند.
به هنگام واکنشهای هیدروژناسیون، همچون تولید کره مارگارین، از ترکیبات آلیفلزی استفاده میشود.
در سنتز ترکیبات آلی، از این مواد به عنوان ریجنت و کاتالیزور بهره میگیرند و همچنین، کمپلکسهایی که از ترکیبات آلیفلزی بدست میآیند، در سنتز بسیاری از ترکیبات آلی کاربرد دارند.
با مواردی که در بالا مطرح شد، اهمیت این نوع از ترکیبات بیشتر روشن میشود اما ترکیبات آلیفلزی برای محیط زیست زیانبار هستند که سبب بوجود آمدن نگرانیهای بسیاری در این زمینه شده است.